신경성기립저혈압의 치료
Treatment of Neurogenic Orthostatic Hypotension
Article information
Trans Abstract
Orthostatic hypotension (OH) is a common feature of sympathetic autonomic dysfunction and can lead to lightheadedness, weakness, dizziness, and syncope. It is defined as decrease in systolic blood pressure of at least 20 mm Hg or diastolic blood pressure of at least 10 mm Hg within 3 minutes of standing. OH is associated with an increased incidence of cerebrovascular disease, myocardial infarction, and mortality. Non-pharmacological treatments may alleviate OH-related symptoms; however, are not sufficient when used alone. Pharmacological treatment is essential in managing OH. In this review, we aimed to discuss non-pharmacological and pharmacological treatment options for OH.
서 론
기립어지럼(orthostatic dizziness)은 앉거나 바로 누운 상태에서 빠르게 일어설 때 현기증, 어지럼이 발생하고, 다시 앉거나 누우면 호전되는 증상이다[1]. 일반적으로 일어설 때 500–1,000 mL의 혈류가 복부나 하지 정맥으로 이동하게 된다. 이에 따라 수축기, 이완기 혈압의 감소와 심장으로의 정맥 환류량(venous return)이 줄어들게 되며 일시적으로 심박출량과 혈압이 감소한다. 정상적으로는 기립 시에 자율신경계, 심혈관계, 내분비계의 보상기전이 일어나 심박 수가 빨라지고 말초혈관저항성이 커져 정맥 환류량을 증가시킨다[2].
기립저혈압(orthostatic hypotension, OH)은 기립어지럼의 중요한 원인 중의 하나로 누워 있다가 일어서서 또는 60°이상의 경사대 검사에서 3분 이내에 수축기 혈압이 20 mm Hg이상 또는 이완기 혈압이 10 mm Hg 이상 떨어지는 경우로 정의한다[3]. 정상적으로 기립 시에 일시적으로 수축기 혈압은 10–15 mm Hg, 이완기 혈압은 5–10 mm Hg 정도 저하될 수 있으며 맥박은 분당 10–25회 증가할 수 있다. 자율신경장애 등의 원인에 의해 심박출량-말초혈관저항성의 부조화가 나타날 경우 이러한 정상적 혈압저하가 과장되게 나타날 수 있다[4]. 기립저혈압의 유병률은 지역사회 인구의 5%–30%로 알려져 있으며[5,6], 요양원 또는 병원 환자 대상으로 41%–50%까지도 보고되고 있다[7,8]. 다양한 원인에 의하여 기립저혈압이 나타날 수 있으며, 임상에서는 흔히 탈수, 또는 전립선약, 혈압약 등의 약물에 의한 경우가 많다(Table 1) [9,10]. 신경성 기립저혈압(neurogenic OH)은 자율신경 기능 부전으로 인하여 나타나는 것으로 말초신경병(당뇨병성 또는 자가면역성 자율신경병 등)이나 중추성 병변(파킨슨병, 다계통위축증 등)과 동반하여 나타나는 것을 말한다[11].
기립저혈압은 일시적으로 뇌 혈류가 감소하는 것으로 기립어지럼뿐만 아니라, 전신쇠약, 심할 경우 의식소실을 일으킬 수 있으며[12], 심혈관질환 이환율과 사망률을 높이는 것으로 알려져 있다[13]. 적절한 치료는 어지럼 개선뿐만 아니라, 우울감을 해소하고 삶의 질을 높일 수 있으며, 기립저혈압과 동반된 위험성과 사망률을 낮출 수 있어 중요하다.
기립저혈압의 치료 목적은 단순히 기립 시 혈압저하를 방지하는 것뿐만 아니라 누운 자세에서 고혈압이 생기지 않으면서 기립 시 발생하는 증상과 실신, 낙상위험을 줄여서 삶의 질을 개선하는 데에 있다. 즉 기립저혈압의 동반증상을 완화하면서, 누운 자세에서 혈압이 180/110 mm Hg을 넘지 않도록 하고 있다[14].
본 종설에서는 신경성기립저혈압환자에서 적절한 비약물성과 약물성 치료에 대하여 논하고자 한다.
본 론
1. 비약물성 치료
혈압은 아침-저녁 시간, 식사, 온도 등에 따라 변하기 때문에 약물치료 단독으로는 부족한 경우가 많으며, 비약물성 치료를 먼저 시도하거나 병행하는 것이 필요하다[11]. 몇 가지 비약물성 치료가 연구되었으나, 환자 증상, 기저질환 등에 따라 개별적으로 선택하여야 하며, 환자 교육 또한 중요하다.
1) 행동치료 및 운동
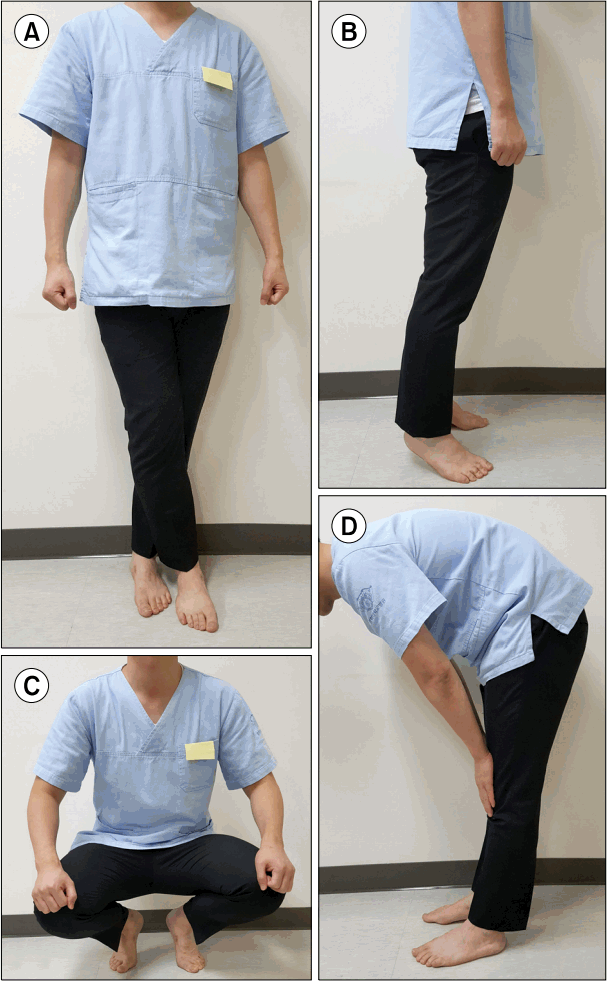
우선 서서히 일어나도록 교육하는 것이 필요하다. 기립시 가슴까지 고개를 숙인 채 일어나면 복부를 압박하여 정맥환류량을 증가시킬 수 있다[15]. 침대에서 일어날 때도 바로 일어나지 않고 침대에 수 분간 앉았다가 서서히 일어나는 게 좋다. 가능하다면 무리하지 않도록 운동하는 것이 좋으며 하지 근육 수축을 증가시키는 운동이 정맥환류량을 늘려 도움을 줄 수 있다. 다리 근육 수축하기, 발등 굽힘, 다리를 꼬고 일어나기[16], 웅크림(squatting) 등이 추천된다(Fig. 1) [11,15,17]. 심한 기립저혈압이 있는 노인의 경우 지팡이를 사용하는 것도 도움이 된다.
2) 압박스타킹
일부 환자에서 압박스타킹으로 기립저혈압과 동반된 증상을 호전시킬 수 있다. 발목 압력 40–60 mm Hg, 엉덩이 압력 30–40 mm Hg로 평균 압력 30 mm Hg 이상으로 조이는 스타킹이 기립 시 혈압저하와 동반증상을 호전시킨다는 보고가 있으며, 압박스타킹을 착용한 환자 60% 이상에서 큰 불편감 없이 착용하였다[18]. 또한, 복대는 복부정맥으로 혈류가 몰리는 것을 줄여 도움이 되며, 정맥혈전방지 스타킹이 일반적으로 흔히 사용되지만, 경한 기립저혈압에서만 연구되었다[19].
3) 수분, 염분 섭취 및 식이조절
일반적으로 하루 1.5–2 L의 물을 섭취하도록 권유하며 충분한 염분 섭취도 필요하다. 환자의 기저 질환을 고려하여 문제가 없다면 식사 중 소금을 첨가하거나 0.5–1 g의 소금을 추가로 섭취하도록 한다. 염분 부족이 원인인지 파악하려면 24시간 소변 나트륨 농도를 측정하여 판정할 수 있으며, 170 mmol 이하인 경우 나트륨 1–2 g을 하루 2–3회 복용하는 것이 도움이 된다[20]. 하지만 염분, 수분보충만으로는 기립저혈압 치료에 부족할 수 있다[21]. 물을 500 mL 정도 마시면 30분 후 교감신경 활동이 증가하여 2시간 동안 수축기 혈압을 20 mm Hg 정도 높인다고 알려져 있으나[22], 자율신경장애가 있는 기립저혈압 환자에서 효과가 있는지에 대해서는 논란의 여지가 있다. 머리를 10–20 cm정도 올려서 자면 신장 혈류량을 줄이고 밤중 이뇨작용을 줄여주어 효과가 있다는 보고가 있으나 증거가 충분하지 않다. 식사는 적은 양을 자주 복용하는 것이 필요하며 고탄수화물 식사와 술은 피하는 것을 추천한다.
2. 약물성 치료
비약물성 치료에도 증상이 지속된다면 약물치료를 시작할 수 있다. 흔히 사용하는 약물은 미도드린(midodrine), 피리도스티그민(pyridostigmine), 플루드로코티손(fludrocortisone)이 있다.
1) 미도드린(midodrine, Midron)
(1) 기전
미도드린은 섭취시에 활성 대사산물인 desglymidodrine으로 대사되어 직접 알파1 아드레날린 수용체(alpha 1 adrenoreceptor)를 활성화하게 되며, 이는 말초 혈관저항성을 높여 하지, 복부 정맥으로 혈류를 줄이고 혈압을 유지한다[23,24]. 미도드린은 무작위비교 임상시험에서 효과가 검증되어 처음으로 기립저혈압에 대하여 미국식품의약국(Food and Drug Administration, FDA)의 승인을 받은 약물이다.
(2) 용량
처음 2.5–5 mg 하루 2–3차례 복용하는 것으로 시작할 수 있으며 최대 10 mg 하루 3차례까지 사용할 수 있다. 최소 효능 용량은 5 mg이지만 이전 연구에 따르면 10 mg에서 효과가 있다고 알려져 있다. 미도드린의 효능은 30분–1시간 사이 나타나며 4시간까지 지속되며 작용시간이 길지 않다.
2) 피리도스티그민(pyridostigmine, Mestinon)
(1) 기전
자율신경절에서 신경전달은 아세틸콜린으로 이루어지기 때문에 항콜린에스테라아제(anticholinesterase)인 피리도스티그민은 아세틸콜린을 증가시켜 자율신경절 신호전달을 증진시킬 수 있다. 자율신경계 압력반사(baroreflex)는 기립 시에 주로 작용하며, 바로 누운 자세에서는 거의 나타나지 않기 때문에 이론적으로 피리도스티그민 효과는 기립 시에만 작용하게 되며 누운 자세고혈압이 나타나지 않으면서 기립 시 혈압저하를 완화할 수 있다[30]. 피리도스티그민은 기립저혈압에 대하여 FDA와 국내에서 승인되지 않아 허가 외로 사용한다.
(2) 용량
처음 30 mg 하루 2–3번으로 시작할 수 있으며, 60 mg 하루 3번까지 증량할 수 있다.
(3) 부작용
콜린성 기전으로 인한 설사, 메스꺼움, 구토가 있고 근육경련 등이 나타날 수 있다. 드물지만 방실차단(atrioventricular block)이 나타날 수 있어 부정맥 환자에서 주의해야 하며, 신기능 장애, 천식과 같은 호흡기 장애 환자에서 주의해야 한다[14].
3) 플루드로코르티손(fludrocortisone, Florinef)
(1) 기전
합성 광물코르티코이드(mineralocorticoid)로 신장에서 나트륨 재흡수를 촉진시켜 혈장량을 증가시키고 알파 아드레날린수용체의 민감도를 증가시켜 혈관수축제에 보완적인 역할을 할 수 있다[14,37]. 플루드로코르티손 또한 기립저혈압에 대하여 FDA와 국내에서 승인되지 않아 허가외로 사용한다.
(2) 용량
처음 하루 0.1 mg 하루 1회부터 하루 0.3 mg까지 증량할 수 있다. 최고 용량은 하루 1 mg으로 알려져 있으나 0.3 mg이상의 용량은 부작용이 심하여 추천하지 않는다[38].
(3) 부작용
플루드로코티손 또한 누운자세고혈압이 나타날 수 있으며 특히 저칼륨혈증이 높은 용량에서 흔히 나타난다. 또한 체중증가, 부종이 나타날 수 있으며 심부전, 신부전, 고혈압 환자에서 사용할 때 주의가 필요하다[14].
4) 기타 약물성 치료
노르에피네프린(norepinephrine) 전구체인 드록시도파(droxidopa)가 2014년 원발자율신경부전(primary autonomic failure), 비당뇨병성자율신경병으로 인한 기립저혈압에 대한 치료제로 FDA의 승인을 받았으며 초기 100 mg 하루 3차례 복용하며 최대 600 mg 하루 3차례까지 복용할 수 있다. 최근 드록시도파의 효능성을 보고하는 메타연구도나와 치료 1주차에 기립저혈압 증상과 기립 시 수축기 혈압저하의 감소를 보고하였다[39]. 이 외에 요힘빈(yohimbine) [32], 인도메타신(indomethacin), 소마토스타틴(somatostatin) 등의 약제가 연구되고 있다[14].
3. 기립저혈압과 누운자세고혈압
자율신경장애 환자에서는 압력반사작용이 손상되어 혈압변동이 크기 때문에 바로누운 자세에서 고혈압이 흔히 동반된다. 원발자율신경부전과 다계통위축증 환자의 절반 가량에서 누운자세고혈압이 동반된다고 알려져 있다[40]. 또한 기립저혈압에 대한 치료제는 혈압을 높이는 작용을 하기 때문에 모든 신경성기립저혈압 환자에서 누운자세고혈압 여부를 평가하여야 한다. 일반적으로 누운 자세고혈압은 바로 누운 자세에서 수축기 혈압 150 mm Hg 이상 또는 이완기 혈압 90 mm Hg 이상으로 정의한다. 하지만 일반적으로 고혈압은 장기적으로 건강에 영향을 주지만, 기립저혈압의 경우 즉각적인 영향을 주기 때문에 기립저혈압 치료를 우선하는 경향이 있다. 따라서 전문가들은 기립저혈압 환자에서 증상 호전이 있을 경우 수축기혈압 160 mm Hg까지는 치료 없이 보는 경우가 많다[10].
1) 비약물성 치료
누운자세고혈압에 대한 가장 좋은 치료는 예방이다. 적어도 낮시간 동안 바로누운 자세를 최대한 피하는 것을 추천하며, 수면 중 최대한 머리를 높게 유지하여 자도록 교육해야 한다[41]. 잠들기 전 고탄수화물 간식을 먹거나 약한 혈관이완제인 포도주 등도 도움이 될 수 있다. 잠들기 1시간 전 수분 섭취는 자제하는 것이 좋다. 또한 미도드린과 플루드로코르티손은 잠들기 4시간 내에는 복용하지 말아야 한다[14].
2) 약물성 치료
수축기혈압 160–180 mm Hg, 이완기혈압 90–100 mm Hg 이상의 누운자세고혈압에서는 개인 특성에 따라 속효성 혈압약을 사용을 고려할 수 있다. 수축기혈압 180 mm Hg 또는 이완기혈압 110 mm Hg 이상의 심한 누운자세고혈압에서는 속효성 고혈압 약제를 저녁에 사용할 수 있으며, 이러한 환자에서는 기립저혈압도 심한 경우가 많아 낙상을 방지하기 위하여 밤중에 화장실 가는 것에 대한 주의가 필요하다. 약물은 취침 전 Losartan 50 mg, Captopril 25 mg, 또는 Hydralazine 25 mg을 사용할 수 있다[10,42].
결 론
신경성기립저혈압의 치료는 환자 특성에 따라 개별화되어야 하며, 일반적으로 운동, 압박스타킹 등의 비약물성 치료와 약물성 치료를 병행해야 한다. 기립저혈압에 대한 약물은 아직까지는 사용근거가 부족하지만 최근 미도드린에 대한 추가 임상시험이 진행 중이며, 드록시도파에 대한 연구도 시행되고 있다. 신경성기립저혈압의 경우 누운자세고혈압이 동반되는 경우가 많아 이에 대한 평가와 예방요법이 추천되며 심한 누운자세 고혈압이 나타날 경우 속효성 혈압강하제 투여에 대한 고려가 필요하다.
Notes
No potential conflict of interest relevant to this article was reported.